Kalsiy va magniy
AI Xulosa
Mavzuni ochishKalsiy va magniy — ishqoriy-yer metallar
Kalsiy va magniy birikmalari qurilish materiallari (sement, ohak), tibbiyot (suyaklar, tishlar mustahkamligi) va qishloq xo'jaligida (tuproq tuzilishi) muhim ahamiyatga ega.
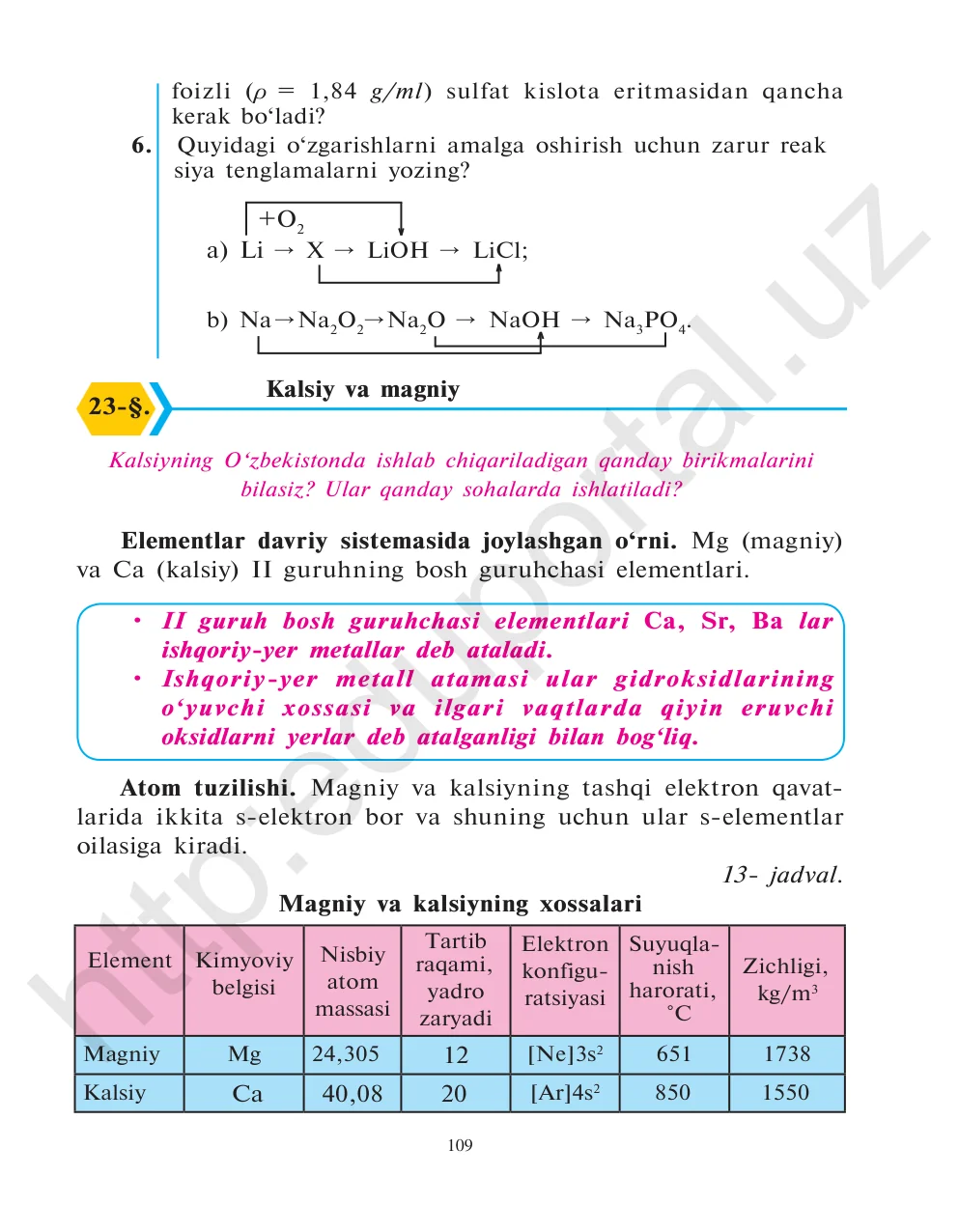
- Atom tuzilishi: II guruh bosh guruhchasi. Tashqi qavatida 2 ta s-elektron. Mg — [Ne]3s², Ca — [Ar]4s². Birikmalarida +2 oksidlanish darajasini namoyon qiladi.
- Tabiatda tarqalishi: Magnezit MgCO₃, dolomit CaCO₃·MgCO₃, kalsit CaCO₃, gips CaSO₄·2H₂O, flyuorit CaF₂. Yer qobig'ida Mg — 3,35%, Ca — 3,5%.
- Kimyoviy xossalari: Suv bilan: Ca + 2H₂O = Ca(OH)₂ + H₂↑ (faol). Mg iliq suv bilan sekin reaksiya qiladi. Kislorod bilan: 2Mg + O₂ = 2MgO (yorqin oq alanga).
- Biologik ahamiyati: Kalsiy — suyak va tishlar tarkibi (Ca₃(PO₄)₂). Magniy — xlorofill molekulasining markazi. Inson organizmida nerv va mushak faoliyatida zarur.
Asosiy atamalar: ishqoriy-yer metallar kalsiy magniy ohaktosh gips
⚠ USTOZ DIQQAT QILING
O'quvchilar magniy va kalsiyni bir xil faollikda deb o'ylashadi. Aslida kalsiy magniydan ancha faol — kalsiy sovuq suv bilan reaksiyaga kirishadi, magniy esa faqat qaynoq suv bilan sekin reaksiya qiladi.
TAJRIBA
Magniy lentasini yoqing (faqat o'qituvchi nazoratida!) — u yorqin oq alanga bilan yonadi. Bu reaksiya: 2Mg + O₂ = 2MgO. Magniy alangasi shu qadar yorqinki, uni to'g'ridan-to'g'ri qarash ko'zga zarar. Ilgari fotoapparatlarda flash sifatida ishlatilgan.
Interaktiv o'yinlar
O'ynash uchun tizimga kiring